MBK - Genetikai Főosztály - Gazda-patogén Interakció és Mikrobiális Genomika Csoport
Kutatási terület
A baktériumok változékonysága és az ebből fakadó igen gyors evolúciójuk komoly kihívást jelent a kutatók, valamint a mezőgazdaság, a humán és állategészségügy és a környezetvédelem szereplői számára is. A genomi szigetek, plazmidok és más mobilis genetikai elemek meghatározó szerepet játszanak a patogenitási faktorok és az antibiotikum rezisztencia gének terjedésében, ezáltal a bakteriális adaptáció és evolúció folyamataiban. Kutatásaink célja ezen folyamatok detektálása, molekuláris mechanizmusaik és szabályozásuk megismerése klasszikus és molekuláris genetikai módszerekkel, valamint genomikai megközelítéssel. Kiemelt figyelmet fordítunk a számos patogén Salmonella serovariáns és más baktériumok (Proteus, Acinetobacter, Morganella) multirezisztenciájáért felelős Salmonella genomi sziget és a horizontális terjedését segítő IncC csoportba tartozó, szintén multirezisztenciát okozó plazmidok kapcsoltarendszerének molekuláris alapjaira és ennek szabályozási folyamataira. Emellet kutatásaink kiterjednek olyan Salmonella serovariánsokra is, melyek terjedése napjainkban zajlik és potenciálisan patogénné válhatnak. Kutatásainkra alapozva olyan baktériumtörzsek fejlesztését is kívánatosnak tartjuk, amelyek akár az ipar, a mezőgazdaság, az állategészségügy és a környezetvédelem területén is alkalmazást nyerhetnek.
Kutatási témák
- A Salmonella genomi sziget 1 genetikája, evolúciója és horizontális terjedése.
- Harmadik generációs szekvenáló rendszer tesztelése
- Antibiotikum rezisztens baktériumok kialakulása és a transzpozíció kapcsolata.
- Multirezisztens Salmonella Infantis törzsek genomanalízise, evoluciója és patogenetikai profilja
A Salmonella genomi sziget 1 genetikája, evolúciója és horizontális terjedése.
A genomi és patogenitási szigetek tekintélyes hányadát teszik ki a prokarióták un. járulékos genomjának. E szigetek mobilitásukkal és genetikai felépítésük változékonyságával jelentősen hozzájárulnak a bakteriális genomok plaszticitásához, ezen keresztül a baktériumok gyors evolúciójához.
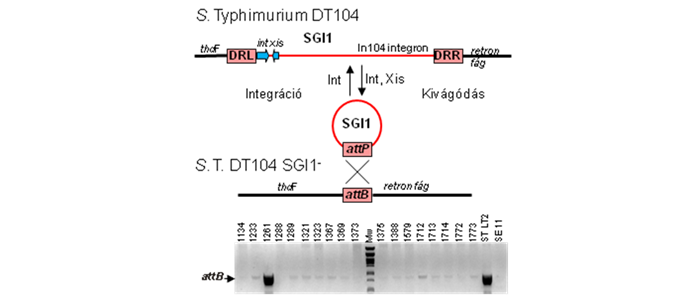
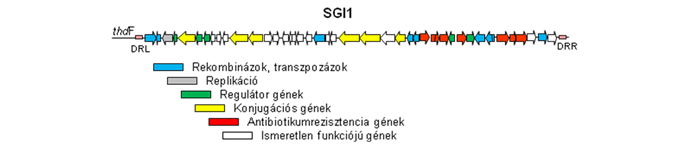
Az 1990-es években világszerte elterjedt multirezisztens Salmonella Typhimurium törzsekben azonosított Salmonella genomi sziget 1 (SGI1) kiváló modellje a genomi szigetek kutatásának. Az SGI1 és variánsai mára számos patogén Salmonella szerovariánsban, Proteus mirabilis, Acinetobacter baumannii és Morganella morganii törzsben megjelentek, így komoly humán- és állategészségügyi kockázatot jelentenek. Mindezek ellenére az SGI1 horizontális terjedésének molekuláris mechanizmusai és a sziget-gazda baktérium kapcsolatok jórészt felderítetlenek.
Kutatásaink az SGI1 horizontális terjedési mechanizmusaira (helyspecifikus rekombináció, konjugáció), az ebben részt vevő IncC plazmidokkal való kooperációjára, valamint a sziget eredetére és evolúciójára (variánsok keletkezése) irányulnak. Emellett tanulmányozzuk a sziget és gazda baktériuma közötti kapcsolatokat, különösen a szigetnek a Salmonella patogenitásában és fitneszében játszott feltételezett szerepét, valamint a sziget terjedését élő állat bélflórájában. A kutatásban partnerünk az MTA ÁOTKI Enterális bakteriológia és alimentáris zoonózis csoportja, valamint az INRA-Université de Tours Infectiologie & Santé Publique, Genomic Plasticity, biodiversity and Antimicrobial Resistance csoportja.
Harmadik generációs szekvenáló rendszer tesztelése
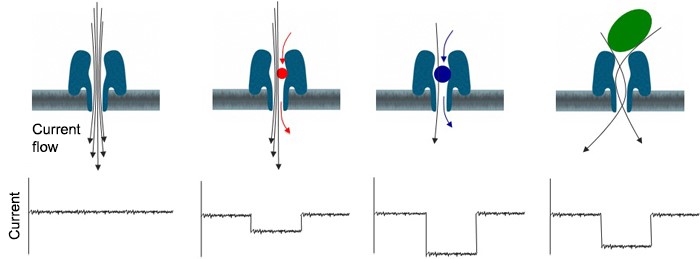
Csoportunk 2014-tól résztvevője az Oxford Nanopore Technologies Ltd. által fejlesztett MinIon szekvenálókészülék teszt programjának (MinIon Access Program – MAP). A készülék alig nagyobb egy pendrive-nál és USB porton keresztül csatlakozik a számítógéphez. A DNS szekvencia leolvasása egy fehérje póruskomplexen való áthaladás közben az átfolyó ionáram változásának detektálásával történik, lényegében egymolekulás szekvenciameghatározás zajlik 512 egyedi csatornán keresztül. A technológia egyik előnye, hogy akár 50100 kb (!) méretű egyedi readeket is képes generálni, ami jelentősen megkönnyíti a szekvenciák kontigokba szervezését.
forrás:Oxford Nanopore, https://www.nanoporetech.com/
Csoportunk a program keretében az IncC plazmidcsalád egyes multirezisztens tagjainak szekvenálását végezte el, melyek ~160-170 kb méretű egykópiás konjugatív plazmidok és igen sok IS elemet hordoznak, ami miatt az új generációs szekvenálási módszerekkel nyerhető 3-400 bp hosszú readekből összeállított kontigok sorrendje nem állapítható meg. A teszt fázisban a MinIon szekvenáló készülékkel nyert hosszú readeket ebben a munkában alkalmaztuk. Reményeink szerint a további fejlesztésekkel párhuzamosan a szekvenálási kapacitások is bővülnek majd és a rendszer a jövőben a genomikai kutatások mindennapos eszközévé válik.
Antibiotikum rezisztens baktériumok kialakulása és a transzpozíció kapcsolata.
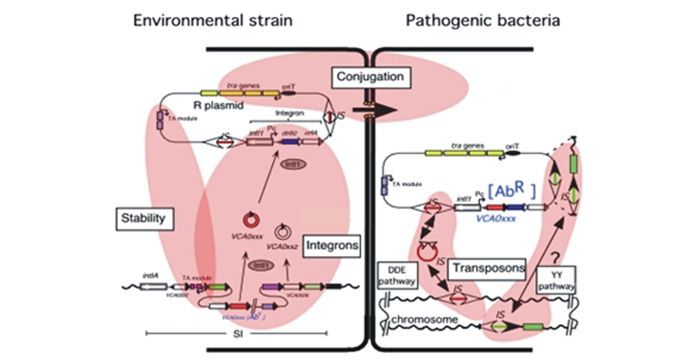
Az inszerciós szekvenciák olyan mobilis elemek, melyek képesek a gazda genomon belül áthelyeződni sőt akár nagyobb léptékű genomátrendeződéseket generálni. Konjugatív plazmidokat és fágokat is érintő átrendeződések révén fontos szerepet játszanak a horizontális géntranszferben, így gyakran az antibiotikum rezisztencia (AR) gének terjedésében is. Az AR kialakulása és a baktériumok közötti gyors továbbadása azóta problémát jelent a gyógyításban, mióta az első antibiotikumok széles körben elérhetővé váltak. Az AR gének elterjedésében az inszerciós szekvenciák, transzpozonok fontos szerepet töltenek be, mivel képesek az AR génekkel együtt olyan vektorokba, pl. konjugatív plazmidokra áthelyeződni, melyek horizontális transzfer révén más baktériumokba is átjuthatnak.
Az AR gének átvitele patogén baktériumokba (az ábra az EU CRAB project alapján készült). Az ábra összefoglalva szemlélteti a rezisztenciagének mobilizálódásának útvonalait: az integron kazetták mozgását és cserélődését, a transzpozíciós mechanizmusokat, a baktériumok közötti konjugációt és az AR-t hordozó plazmidok stabilizálódását.
Transzpozonokkal kapcsolatos kutatásaink nagy része egy Escherichia coliban „honos” IS elemre, az IS30-ra irányul. Az elem transzpozíciója során először egy körré zárt forma keletkezik, majd ez a transzpozon kör integrálódik a cél-DNS-be. A körré zárt elem vég-vég kapcsolódása transzpozáz jelenlétében nagy gyakorisággal okoz inszerciókat, deléciókat és inverziókat. A folyamatok molekuláris szintű feltárásával nyilvánvalóvá vált, hogy ez a „copy out-paste in” mechanizmus a legelterjedtebb az IS elemek körében. Mivel az elem körré zárt formájának képződése egy Holliday-junction-hoz hasonló, de nicket is tartalmazó struktúra megoldódásán keresztül történik, várható, hogy ez a gazda sejt számos repair folyamatára hatással van. Kutatásaink célja ennek a transzpozon-gazdasejt kapcsolatnak a vizsgálata microarray analízis, hálózatelemzés és kísérletes módszerekkel.
Multirezisztens Salmonella Infantis törzsek genomanalízise, evoluciója és patogenetikai profilja (együttműködő partnerként részvétel MTA ÁOTKI Enterális bakteriológia és alimentáris zoonózis csoportja projektjében)
Számos Salmonella törzs az állatorvosi gyakorlatban és a humán egészségügy számára egyaránt komoly kockázatot jelent. Korábbi és jelenlegi vizsgálatok kimutatták, hogy a S. Infantis törzsek a 90-es évek óta jóval szélesebb körű elterjedést mutatnak, ami az izolátumok növekvő gyakoriságú antibiotikum rezisztenciájával is együtt jár. Célunk a rezisztens S. Infantis törzsek gyors és feltehetőleg klonális terjedésének a genetikai hátterét megismerni. Ennek érdekében genomszekvenálásokat hajtottunk végre és vizsgáljuk régi és újonnan izolált törzsek közötti különbségeket. Választ keresünk arra, hogy milyen genetikai átrendeződések állnak az új törzsek terjedésének hátterében (plazmidok, transzpozonok, integronok megszerzése), megjelentek-e új genomi vagy patogenitási szigetek; milyen változások következtek be az újonnan izolált törzsek genomi vagy patogenitási szigeteiben. Az esetleges nagyléptékű különbségek (plazmidok, genomi szigetek megjelenése) vizsgálatára genom manipulációra alkalmas eszközöket fejlesztettünk, melyek alkalmazása választ adhat a felvetett kérdésekre. Ezen kutatások betekintést nyújtanak a rezisztens klónok kialakulásába, evolúciójába és reményeink szerint terjedési sikerük okait is jobban megérthetjük.
A bélbolyhok felszínén megtelepedett baktériumok (Forrás: Dr Nagy Béla, MTA ATK ÁOTI)
Kutatásainkat támogatja:
NKFIH K 128203 Két különböző mobilis multirezisztencia faktor együttműködésének vizsgálata: Az IncA/C plazmidok és az SGI1 típusú genomi szigetek kapcsolata (2018-2022).
OTKA
K 105635 A Salmonella Genomi Sziget 1 (SGI1) molekuláris genetikája és ökológiája: a mobilitás, a terjedés és a patogenetikai jelentőség rejtelmei (2012-2017)
K 101546 Előtérbe nyomuló multirezisztens Salmonella Infantis törzsek evolúciója és pathogenetikai profilja (2012-2016)
Munkatársak

Publikációk
Válogatott tudományos közlemények
Szmolka A, Szabó M, Kiss J, Pászti J, Adrián E, Olasz F, Nagy B (2018) Molecular epidemiology of the endemic multiresistance plasmid pSI54/04 of Salmonella Infantis in broiler and human population in Hungary. Food Microbiol. 71:25-31. doi: 10.1016/j.fm.2017.03.011. http://dx.doi.org/10.1016/j.fm.2017.03.011.
Anna Hegyi, Mónika Szabó, Ferenc Olasz, János Kiss.(2017) Identification of oriT and a recombination hot spot in the IncA/C plasmid backbone. Scientific Reports, Sci Rep. 6;7(1):10595. doi: 10.1038/s41598-017-11097-0
Veress A., Wilk T., Kiss J., Papp P. P., Olasz F. (2017) Two Draft Genome Sequences of Sphingobacterium sp. Strains Isolated from Honey. Genome Announc. 5(48). pii: e01364-17. doi::10.1128/genomeA.01364-17.
Wilk T, Szabó M, Szmolka A, Kiss J, Olasz F, and Nagy B (2017) Genome Sequences of Salmonella enterica subsp. enterica Serovar Infantis Strains from Hungary Representing Two Peak Incidence Periods in Three Decades. Genome Announc. 5: e01735-16.doi:10.1128/genomeA.01735-16
Mónika Szabó, Tibor Nagy, Tímea Wilk, Tibor Farkas, Anna Hegyi, Ferenc Olasz, János Kiss (2016) Characterization of Two Multidrug-Resistant IncA/C Plasmids from the 1960s by Using the MinION Sequencer Device. Antimicrob Agents Chemother 60:6780–6786. doi:10.1128/AAC.01121-16.
Gábor Murányi, Mónika Szabó, Ferenc Olasz, János Kiss (2016) Determination and Analysis of the Putative AcaCD-Responsive Promoters of Salmonella Genomic Island 1. PLoS ONE 11(10): e0164561. doi:10.1371/journal.pone.0164561
Wilk T, Szabó M, Szmolka A, Kiss J, Barta E, Nagy T, Olasz F, Nagy B. (2016) Genome Sequences of Multidrug-Resistant Salmonella enterica subsp. enterica Serovar Infantis Strains from Broiler Chicks in Hungary. Genome Announc. 4(6). pii: e01400-16. doi: 10.1128/genomeA.01400-16.
Kiss, J., Papp, P., P., Szabó, M., Farkas, T., Murányi, G., Szakállas E. and Olasz F. (2015) The master regulator of IncA/C plasmids is recognized by the Salmonella Genomic island SGI1 as a signal for excision and conjugal transfer. Nucleic Acids Res. 43 (18): 8735-8745 doi:10.1093/nar/gkv758
Olasz F., Nagy T., Szabó M., Kiss J., Szmolka A., Barta E., van Tonder A., Thomson N., Barrow P., Nagy B. (2015)Genome Sequences of Three Salmonella enterica subsp. enterica Serovar Infantis Strains from Healthy Broiler Chicks in Hungary and in the United Kingdom. Genome Announc. 3(1). pii: e01468-14. doi: 10.1128/genomeA.01468-14.
Kiss, János,Béla Nagy, Ferenc Olasz,(2012) Stability, entrapment and variant formation of Salmonella genomic island 1. PLo S ONE 7(2): e32497.
Fekete Péter Z., Elzbieta Brzuszkiewicz, Gabriele Blum-Oehler, Ferenc Olasz, Mónika Szabó,Gerhard Gottschalk, Jörg H. Hacker and Béla Nagy (2012) Sequence analysis and comparative pathogenomics of plasmid pTc conferring virulence and antimicrobial resistance for F18+ porcine enterotoxigenic Escherichia coli. Int J Med Microbiol. 2011 Oct 12. [Epub ahead of print] 302, 4-9.
Szabó M., Kiss J., and Olasz F.(2010): Functional organization of the inverted repeats of IS30. J Bacteriol. 2010 Jul;192(13):3414-23. Epub 2010 Apr 23.
Szabó M., Kiss J., Nagy Z.,Chandler M. and Olasz F. (2008): Sub-terminal sequences modulating IS30 transposition in vivo and in vitro. J.Mol.Biol.2008 Jan 11;375(2):337-52. Epub 2007 Oct 23.
Ferg M, Sanges R, Gehrig J, Kiss J,Bauer M, Lovas A, Szabo M,Yang L, Straehle U, Pankratz MJ, Olasz F, Stupka E, Müller F. (2007): The TATA-binding protein regulates maternal mRNA degradation and differential zygotic transcription in zebrafish. EMBO J. Sep 5;26(17):3945-56. Epub 2007 Aug 16;
János Kiss, Zita Nagy,Gábor Tóth, György Botond Kiss, Júlia Jakab, Michael Chandler, Ferenc Olasz:(2007): Transposition and target specificity of the typical IS30 family element IS1655 from Neisseria meningitidis.Molec. Microbiol. 63 (6): 1731-1747 MAR 2007
Nagy Zita,Mónika Szabó,Michael Chandler and Ferenc Olasz(2004): Analysis of the N-terminal DNA binding domain of the IS30 transposase. Molec. Microbiol. 54(2):478-88.
Kiss János, Mónika Szabó and Ferenc Olasz(2003): Site-specific recombination by the DDE-family member IS30 transposase. Proc Natl Acad Sci U S A.(100)25:1500-05.
Olasz Ferenc, Tamás Fischer, Mónika Szabó, Zita Nagy and János Kiss(2003).: Gene conversion in transposition of Escherichia coli elementIS30. J. Mol. Biol. 334/5 967-978.
Szabó Mónika,Ferenc Müller, János Kiss,Carolin Balduf, Uwe Strähle and Ferenc Olasz(2003): Trans-kingdom transposition and gene targeting mediated by the prokaryotic mobile element IS30FEBS Lett. 550(1-3):46-50.
Nagy, Z. Szeverényi, I. Farkas, T. Olasz, F. and Kiss J.(2003): Detection and analysis of transpositionally active head-to-tail dimers in three additional E. coliIS elements. Microbiology 149: 1297-1310
Kiss, J. and Olasz, F.(1999): Formation and transposition of the covalently closed IS30 circle: the relation between tandem dimers and monomeric circles. Molec. Microbiol. 34(1) 37-52
Olasz, F., Kiss, J.,König, P., Buzás, Zs., Stalder, R. and Arber W. (1998): Target specificity of insertion element IS30. Molec. Microbiol. 28(4) 691-704
Olasz, F., Farkas, T., Kiss, J.,Arini, A. and Arber W. (1997): Terminal inverted repeats of insertion sequence IS30 serve as target for transposition. J. Bacteriol. 179:7551-7558
Farkas, T, Kiss J, Olasz F(1996) The construction and characterization of an effective transpositional system based on IS30. FEBS Letters 390:53-58
Szabadalom
Mónika Szabó, János Kiss, Ferenc Olasz, (ABC, Gödöllő, Hungary), Ferenc Müller, Lászlo Tora, Uwe Strähle (IGBMC, Strasbourg, France). European Patent application, No 01402754.4. Site-directed recombinase fusion proteins and corresponding polynucleotides, vectors and kits, and their uses for site-directed DNA recombination.
Programajánló
Hírek
Tisztelt Látogatók!
A hazai agrár-felsőoktatás szükséges megújulásának mérföldköve az alapítványi fenntartású Magyar Agrár- és Élettudományi Egyetem (MATE) létrejötte, amely 2021. február 1-től 5 campuson, több mint 13 ezer hallgató számára fogja össze a dunántúli és közép-magyarországi élettudományi és kapcsolódó képzéseket. Az intézményhez csatlakozik a Nemzeti Agrárkutatási és Innovációs Központ (NAIK) 11 kutatóintézete is, így az új intézmény nem csupán egy oktatási intézmény lesz, hanem az ágazat szellemi, szakpolitikai és innovációs központjává válik, amely nagyobb mozgásteret biztosít a képzések, a gazdálkodás és szervezet modernizálásához, fejlesztéséhez. Az összeolvadással magasabb fokozatra kapcsolunk, a kutatói és egyetemi szféra szorosabban fonódik majd össze, aminek következtében még több érdekes, izgalmas kutatás-fejlesztés születhet majd az agrárium területén.
Kérjük, kövesse tevékenységünket a jövőben is a www.uni-mate.hu honlapon!
2021. február 1-től a Nemzeti Agrárkutatási és Innovációs Központ 11 kutatóintézete, köztük az MBK is a Szent István Egyetemmel együtt Magyar Agrár- és Élettudományi Egyetem néven, közhasznú magán felsőoktatási intézményként,átalakított szervezeti struktúrával folytatja tovább működését.